Druga edycja konferencji „Arena Jakości: Odkrywamy Tajemnice Bezpiecznej Żywności” odbyła się w dniach 19–20 marca 2026 r. w Cukrowni Żnin. Wydarzenie zgromadziło przedstawicieli branży spożywczej, ekspertów laboratoriów oraz specjalistów ds. jakości, koncentrując się na praktycznych aspektach bezpieczeństwa żywności.
Były to dwa dni intensywnych prelekcji, warsztatów i wymiany doświadczeń, ukierunkowanych nie na teorię, ale na konkretne problemy operacyjne w firmach produkcyjnych i dystrybucyjnych.
Od etykiety po laboratorium
Jednym z kluczowych tematów było znakowanie żywności. Prelegenci pokazywali realne rozbieżności w tabelach wartości odżywczych między rynkami oraz najczęstsze błędy producentów. Wątek „clean label” został sprowadzony do praktyki: jako wyzwanie technologiczne i ryzyko nieprecyzyjnej komunikacji, a nie tylko trend marketingowy.
Równolegle dużo uwagi poświęcono bezpieczeństwu łańcucha dostaw. Omawiano konkretne przypadki food fraud, sposoby wykrywania nieautentycznych surowców oraz narzędzia ograniczania ryzyka nadużyć.
Twarde dane i trudne analizy
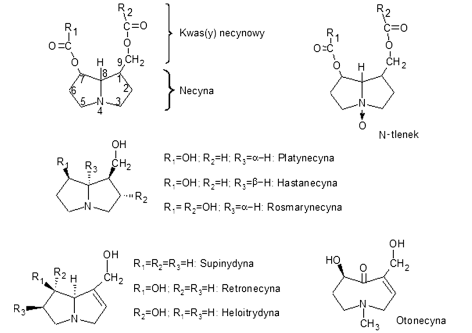
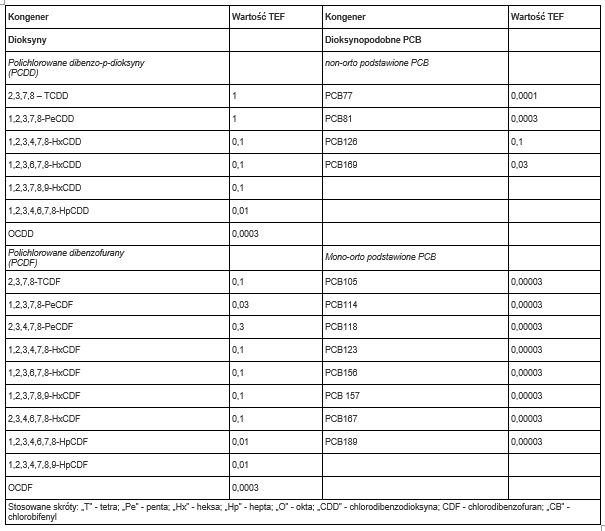
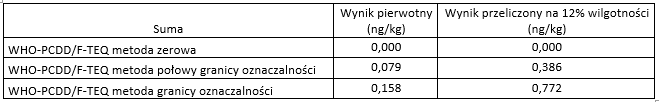
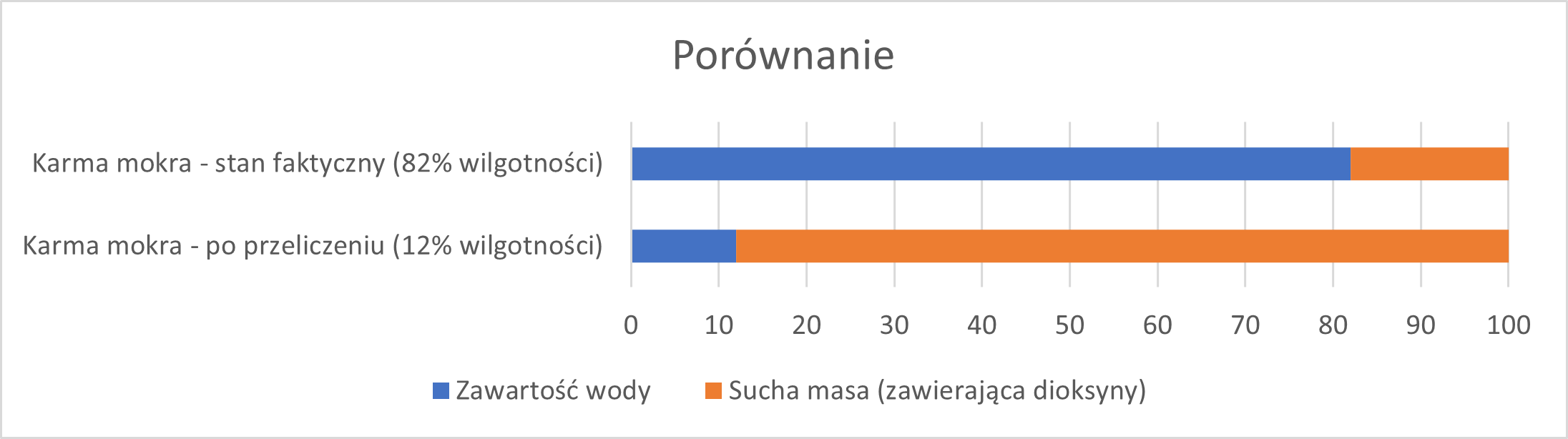
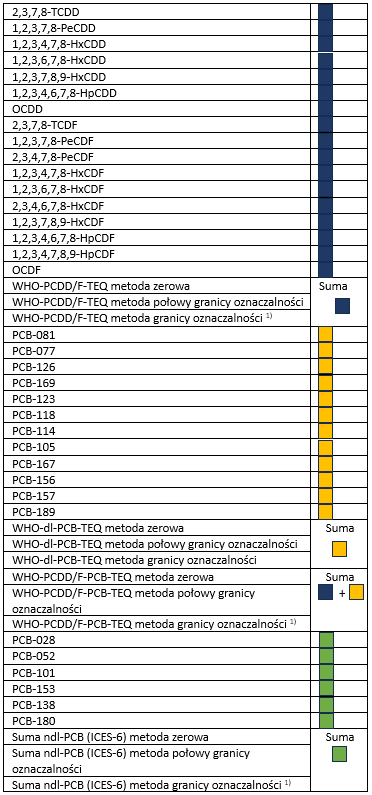
Silnym filarem konferencji była analityka laboratoryjna. Uczestnicy mogli prześledzić proces badań migracji z opakowań – od doboru warunków po interpretację wyników. Uzupełnieniem były zagadnienia wymagające zaawansowanych metod, takie jak oznaczanie dioksyn czy pozostałości pestycydów.
Nie zabrakło też tematów mikrobiologicznych. Warsztat poprowadzony przez Małgorzatę Stachowiak pokazał, gdzie w praktyce „ukrywają się” źródła skażeń w zakładach i jak skutecznie je eliminować: między innymi biorąc pod uwagę błędy higieniczne oraz niewłaściwie zaprojektowane procesy mycia.
Analiza sensoryczna i badania konsumenckie
Duże znaczenie miały także prelekcje dotyczące jakości z perspektywy konsumenta. Uczestnicy poznali metody analizy sensorycznej oraz interpretacji badań konsumenckich, które pozwalają ocenić, jak produkt jest odbierany na rynku. Dzięki temu firmy mogą lepiej dopasować receptury, etykiety i komunikację do oczekiwań klientów.
Alergeny w praktyce
Wystąpienie Małgorzaty Krzepkowskiej poświęcone alergenom obejmowało zagrożenia związane z zanieczyszczeniami krzyżowymi, strategie zarządzania alergenami w zakładach produkcyjnych oraz praktyczne metody kontroli, w tym monitorowanie i oznakowanie produktów. Uczestnicy mogli poznać sposoby minimalizowania ryzyka dla konsumentów i spełniania wymogów prawnych.
RASFF i zarządzanie kryzysowe
Istotnym punktem programu była prelekcja gościa specjalnego, lek. wet. Jacka Kucharskiego, poświęcona systemowi RASFF – europejskiemu Systemowi Wczesnego Ostrzegania o Niebezpiecznej Żywności i Paszach. Wystąpienie koncentrowało się na praktycznym wykorzystaniu systemu w zarządzaniu ryzykiem oraz na tym, jak firmy powinny reagować na zgłoszenia i incydenty.
Omówiono między innymi:
• mechanizm działania systemu i przepływ informacji,
• najczęstsze przyczyny zgłoszeń,
• konsekwencje dla producentów i dystrybutorów,
• dobre praktyki w zakresie szybkiego reagowania i komunikacji kryzysowej.
Audyty okiem praktyka
Wystąpienie Zbigniewa Oczadłego, eksperta Centrum Jakości AgroEko oraz QA Solutions, dotyczące audytów jasno wskazywało jedno: liczą się dowody. Prelegent skupił się na tym, jak przygotować dokumentację, jakich niezgodności unikać i co faktycznie decyduje o wyniku audytu.
II edycja Areny Jakości pokazała, że branża potrzebuje praktyki, a nie deklaracji. Program wydarzenia obejmował cały wachlarz realnych wyzwań – od etykiet, przez badania laboratoryjne i analizy sensoryczne, po zarządzanie ryzykiem i alergenami w produkcji. To konferencja, która zamiast opisywać wyzwania, pokazała, jak sobie z nimi radzić.
Na zakończenie konferencji odbył się konkurs, w którym z przymrużeniem oka sprawdzono poziom wiedzy uczestników z poruszonych zagadnień. Zwycięzcy otrzymali nagrody w postaci bezpłatnych szkoleń J.S. Hamilton oraz dwudniowego pobytu w Cukrowni Żnin. To wydarzenie pokazało, że nauka i dobra zabawa mogą iść w parze!
Zachęcamy do zapoznania się z poniższą fotorelacją z wydarzenia.